ORBITAL DAN PERANANNYA DALAM IKATAN KOVALEN
a.Sifat - sifat gelombang
1. Dipantulkan (Refleksi)
Tentunya sahabat sudah sangat mengerti tentang pemantulan ini, jadi secara garis besar saya rasa kita sudah sepaham.
Dalam pemantulan gelombang berlaku hukum pemantulan gelombang, yaitu :
- Besar sudut datangnya gelombang sama dengan sudut pantul gelombang.
- Gelombang datang, gelombang pantul, dan garis normal terletak pada satu bidang datar.
2. Dibiaskan (refraksi)
Pembiasan gelombang adalah pembelokan arah rambat gelombang karena melalui medium yang berbeda kerapatannya.
3. Dipadukan (interferensi)
Perpaduan gelombang
terjadi apabila terdapat gelombang dengan frekuensi dan beda fase saling
bertemu. Hasil interferensi gelombang akan ada 2, yaitu konstruktif
(saling menguatkan) dan destruktif (saling melemahkan). Interferensi
Konstruktif terjadi saat 2 gelombang bertemu pada fase yang sama,
sedangkan interferensi destruktif terjadi saat 2 gelombang bertemu pada
fase yang berlawanan.
4. Dibelokkan/disebarkan (Difraksi)
Difraksi gelombang
adalah pembelokkan/penyebaran gelombang jika gelombang tersebut melalui
celah. Geja difraksi akan semakin tampak jelas apabila celah yang
dilewati semakin sempit.
5. Dispersi Gelombang
Dispersi adalah penyebaran bentuk gelombang ketika merambat melalui suatu medium. Dispersi tidak akan terjadi pada gelombang bunyi yang merambat melalui udara atau ruang hampa. Medium yang dapat mempertahankan bentuk gelombang tersebut disebut medium nondispersi.
6. Dispolarisasi (diserap arah getarnya)
Polarisasi adalah
peristiwa terserapnya sebagian arah getar gelombang sehingga hanya
tinggal memiliki satu arah saja. Polarisasi hanya akan terjadi pada
gelombang transversal, karena arah gelombang sesuai dengan arah
polarisasi, dan sebaliknya, akan terserap jika arah gelombang tidak
sesuai dengan arah polarisasi celah tersebut.
b. Orbital ikatan dan orbital anti ikatan
Menurut
teori orbital molekul, orbital molekul dihasilkan dari interaksi antara
dua atau lebih orbital atom. Terjadinya tumpang tidih suatu orbital
mengarah pada pembentukan dua orbital atom : satu orbital molekul ikatan
dan satu orbital molekul antiikatan. Orbital molekul ikatan (bonding
molecular orbital) memiliki energi yang lebih rendah dan kestabilan yang
lebih besar dibandingkan dengan orbital atom pembentuknya. Orbital
molekul antiikatan (antibonding molecular orbital) memiliki energi yang
lebih tinggi dan kestabilan yang lebih rendah dibandingkan dengan
orbital-orbital atom pembentuknya.
c. Orbital hibrita karbon
Hibrid sp3
Hibridisasi menjelaskan atom-atom yang berikatan dari sudut pandang sebuah atom. Untuk sebuah karbon yang berkoordinasi secara tetrahedal (seperti metana, CH4), maka karbon haruslah memiliki orbital-orbital yang memiliki simetri yang tepat dengan 4 atom hidrogen. Konfigurasi keadaan dasar karbon adalah 1s2 2s2 2px1 2py1 atau lebih mudah dilihat:
(Perhatikan bahwa orbital 1s memiliki energi lebih rendah dari orbital 2s, dan orbital 2s berenergi sedikit lebih rendah dari orbital-orbital 2p)
Teori ikatan valensi memprediksikan, berdasarkan pada keberadaan dua orbital p yang terisi setengah, bahwa C akan membentuk dua ikatan kovalen, yaitu CH2. Namun, metilena adalah molekul yang sangat reaktif (lihat pula: karbena), sehingga teori ikatan valensi saja tidak cukup untuk menjelaskan keberadaan CH4.
Lebih lanjut lagi, orbital-orbital keadaan dasar tidak bisa digunakan untuk berikatan dalam CH4. Walaupun eksitasi elektron 2s ke orbital 2p secara teori mengizinkan empat ikatan dan sesuai dengan teori ikatan valensi (adalah benar untuk O2), hal ini berarti akan ada beberapa ikatan CH4 yang memiliki energi ikat yang berbeda oleh karena perbedaan aras tumpang tindih orbital. Gagasan ini telah dibuktikan salah secara eksperimen, setiap hidrogen pada CH4 dapat dilepaskan dari karbon dengan energi yang sama.
Untuk menjelaskan keberadaan molekul CH4 ini, maka teori hibridisasi digunakan. Langkah awal hibridisasi adalah eksitasi dari satu (atau lebih) elektron:

Proton yang membentuk inti atom hidrogen akan menarik salah satu elektron valensi karbon. Hal ini menyebabkan eksitasi, memindahkan elektron 2s ke orbital 2p. Hal ini meningkatkan pengaruh inti atom terhadap elektron-elektron valensi dengan meningkatkan potensial inti efektif.
Kombinasi gaya-gaya ini membentuk fungsi-fungsi matematika yang baru yang dikenal sebagai orbital hibrid. Dalam kasus atom karbon yang berikatan dengan empat hidrogen, orbital 2s (orbital inti hampir tidak pernah terlibat dalam ikatan) "bergabung" dengan tiga orbital 2p membentuk hibrid sp3 (dibaca s-p-tiga) menjadi

Pada CH4, empat orbital hibrid sp3 bertumpang tindih dengan orbital 1s hidrogen, menghasilkan empat ikatan sigma. Empat ikatan ini memiliki panjang dan kuat ikat yang sama, sehingga sesuai dengan pengamatan.
 sama dengan
sama dengan 
Sebuah pandangan alternatifnya adalah dengan memandang karbon sebagai anion C4−. Dalam kasus ini, semua orbital karbon terisi:

Jika kita menrekombinasi orbital-orbital ini dengan orbital-s 4 hidrogen (4 proton, H+) dan mengijinkan pemisahan maksimum antara 4 hidrogen (yakni tetrahedal), maka kita bisa melihat bahwa pada setiap orientasi orbital-orbital p, sebuah hidrogen tunggal akan bertumpang tindih sebesar 25% dengan orbital-s C dan 75% dengan tiga orbital-p C. HaL ini sama dengan persentase relatif antara s dan p dari orbital hibrid sp3 (25% s dan 75% p).
Menurut teori hibridisasi orbital, elektron-elektron valensi metana seharusnya memiliki tingkat energi yang sama, namun spektrum elektonnya menunjukkan bahwa terdapat dua pita, satu pada 12,7 eV (satu pasangan elektron) dan saty pada 23 eV (tiga pasangan elektron). Ketidakkonsistenan ini dapat dijelaskan apabila kita menganggap adanya penggabungan orbital tambahan yang terjadi ketika orbital-orbital sp3 bergabung dengan 4 orbital hidrogen.
Hibrid sp2
Senyawa karbon ataupun molekul lainnya dapat dijelaskan seperti yang dijelaskan pada metana. Misalnya etilena (C2H4) yang memiliki ikatan rangkap dua di antara karbon-karbonnya. Struktur Kekule metilena akan tampak seperti:
Ethene Lewis Structure. Each C bonded to two hydrogens and one double bond between them.
Dalam hibridisasi sp2, orbital 2s hanya bergabung dengan dua orbital 2p:

membentuk 3 orbital sp2 dengan satu orbital p tersisa. Dalam etilena, dua atom karbon membentuk sebuah ikatan sigma dengan bertumpang tindih dengan dua orbital sp2 karbon lainnya dan setiap karbon membentuk dua ikatan kovalen dengan hidrogen dengan tumpang tindih s-sp2 yang bersudut 120°. Ikatan pi antara atom karbon tegak lurus dengan bidang molekul dan dibentuk oleh tumpang tindih 2p-2p (namun, ikatan pi boleh terjadi maupun tidak).
Jumlah huruf p tidaklah seperlunya terbatas pada bilangan bulat, yakni hibridisasi seperti sp2.5 juga dapat terjadi. Dalam kasus ini, geometri orbital terdistorsi dari yang seharusnya. Sebagai contoh, seperti yang dinyatakan dalam Kaidah Bent, sebuah ikatan cenderung untuk memiliki huruf-p yang lebih banyak ketika ditujukan ke substituen yang lebih elektro negatif.
Hibrid sp
Ikatan kimia dalam senyawa seperti alkuna dengan ikatan rangkap tiga dijelaskan dengan hibridisasi sp.
Dalam model ini, orbital 2s hanya bergabung dengan satu orbital-p, menghasilkan dua orbital sp dan menyisakan dua orbital p. Ikatan kimia dalam asetilena (etuna) terdiri dari tumpang tindih sp-sp antara dua atom karbon membentuk ikatan sigma, dan dua ikatan pi tambahan yang dibentuk oleh tumpang tindih p-p. Setiap karbon juga berikatan dengan hidrogen dengan tumpang tindih s-sp bersudut 180°.
Hibridisasi dan bentuk molekul
Hibridisasi membantuk kita dalam menjelaskan bentuk molekul:| Jenis molekul | Utama kelompok | Logam transisi |
|---|---|---|
| AX2 |
|
|
| AX3 |
|
|
| AX4 |
|
|
| AX5 | - |
|
| AX6 | - |
|
 , maka berlaku: 1 +
, maka berlaku: 1 +  i
i j cos(
j cos( ) = 0. Rasio p/s untuk hibrid i adalah
) = 0. Rasio p/s untuk hibrid i adalah  i2, dan untuk hibrid j
i2, dan untuk hibrid j  j2. Dalam kasus khusus hibrdid dengan atom yang sama, dengan sudut
j2. Dalam kasus khusus hibrdid dengan atom yang sama, dengan sudut  , persamaan tersebut akan tereduksi menjadi 1 +
, persamaan tersebut akan tereduksi menjadi 1 +  2 cos(
2 cos( ) = 0. Sebagai contoh, BH3 memiliki geometri datar trigonal, sudut ikat 120o, dan tiga hibrid yang setara. Maka 1 +
) = 0. Sebagai contoh, BH3 memiliki geometri datar trigonal, sudut ikat 120o, dan tiga hibrid yang setara. Maka 1 +  2 cos(
2 cos( ) = 0 menjadi 1 +
) = 0 menjadi 1 +  2 cos(120o) = 0, berlaku juga
2 cos(120o) = 0, berlaku juga  2 = 2 untuk rasio p/s. Dengan kata lain terdapat hibrid sp2 seperti yang diperkirakan dari daftar di atas.
2 = 2 untuk rasio p/s. Dengan kata lain terdapat hibrid sp2 seperti yang diperkirakan dari daftar di atas.| molekul hipervalen (Resonansi) | ||
|---|---|---|
| Jenis molekul | Utama kelompok | Logam transisi |
| AX2 | - | Linear (180°) |
 |
||
| AX3 | - | Datar trigonal (120°) |
 |
||
| AX4 | - | Tetrahedral (109.5°) |
 |
||
| Datar persegi (90°) | ||
 |
||
| AX5 | Bipiramida trigonal (90°, 120°) | Bipiramida trigonal, Piramida persegi[7] |
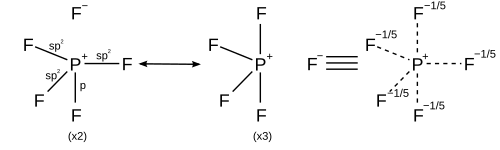 |
||
| AX6 | Oktahedral (90°) | Oktahedral (90°) |
 |
 |
|
| AX7 | Bipiramida pentagonal (90°, 72°) | Bipiramida pentagonal, oktahedral dengan sudut tambahan, Piramida persegi dengan sudut tambahan[8] |
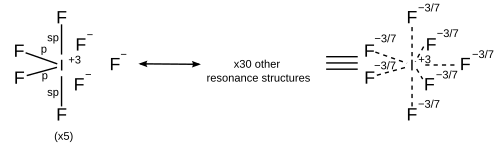 |
||







Komentar ini telah dihapus oleh administrator blog.
BalasHapusApa yang di maksud dengan ikatan kimia
BalasHapusIkatan kimia adalah sebuah proses fisika yang bertanggung jawab dalam interaksi gaya tarik menarik antara dua atom atau molekul yang menyebabkan suatu senyawa diatomik atau poliatomik menjadi stabil. Penjelasan mengenai gaya tarik menarik ini sangatlah rumit dan dijelaskan oleh elektrodinamika kuantum. Dalam praktiknya, para kimiawan biasanya bergantung pada teori kuantum atau penjelasan kualitatif yang kurang kaku (namun lebih mudah untuk dijelaskan) dalam menjelaskan ikatan kimia. Secara umum, ikatan kimia yang kuat diasosiasikan dengan transfer elektron antara dua atom yang berpartisipasi. Ikatan kimia menjaga molekul-molekul, kristal, dan gas-gas diatomik untuk tetap bersama. Selain itu ikatan kimia juga menentukan struktur suatu zat.
HapusKenapa Orbital molekul ikatan (bonding molecular orbital) memiliki energi yang lebih rendah dan kestabilan yang lebih besar dibandingkan dengan orbital atom pembentuknya sedangkan Orbital molekul antiikatan (antibonding molecular orbital) memiliki energi yang lebih tinggi dan kestabilan yang lebih rendah dibandingkan dengan orbital-orbital atom pembentuknya.
BalasHapusMenurut teori orbital molekul, orbital molekul dihasilkan dari interaksi antara dua atau lebih orbital atom. Terjadinya tumpang tidih suatu orbital mengarah pada pembentukan dua orbital atom : satu orbital molekul ikatan dan satu orbital molekul antiikatan. Orbital molekul ikatan (bonding molecular orbital) memiliki energi yang lebih rendah dan kestabilan yang lebih besar dibandingkan dengan orbital atom pembentuknya. Orbital molekul antiikatan (antibonding molecular orbital) memiliki energi yang lebih tinggi dan kestabilan yang lebih rendah dibandingkan dengan orbital-orbital atom pembentuknya.
HapusTolong jelaskan perbedaan antara refraksi dengan interferensi ?
BalasHapus